· 化学 無水酢酸の使い方 化学大辞典だと思いますが、酢酸ニッケルの製造方法として、 無水酢酸に硝酸ニッケル六水和物を溶解すれば酢酸ニッケル が析出するとありました。 無水酢酸は(ch3o)2Oなので 質問noアニリンが無水酢酸と反応したときの変化を化学反応式で示すと, C 6 H 5 NH 2 +(CH 3 CO) 2 O→C 6 H 5 NHCOCH 3 +CH 3 COOH質問:化学反応 ――化学反応―― 前に戻る Q6 チオ硫酸ナトリウムや亜硫酸カルシウム,アスコルビン酸を用いて ①次亜塩素酸ナトリウム水溶液 ②次亜塩素酸カルシウム水溶液 を中和する際の反応. Q2 「スライム電池」の原理. Q0 SO 2 の実験的

15 See How To Solve It At Qanda
アニリン 無水酢酸 化学反応式
アニリン 無水酢酸 化学反応式-融点測定 -アニリンと無水酢酸からアセトアニリドを合成し、再結晶法により精製- 実験日 7月4日金曜日 実験場所 1352材料設計学学生実験室 実験環境 天気:曇り 気温:232℃ 湿度:598% 目的 アニリンと無水酢酸からアセトアニリドを合成し、再結晶法により生成物を精製し、収率を計算する。アニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は For more information and source, see on this link 高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット For more information and source,




高校化学 アニリンの製法 映像授業のtry It トライイット
無水酢酸 chem_idjpn cas rn®1047 化学物質名(和名)無水酢酸 化学物質名(英名)aceticanhydride 分子式c4h6o3Oh 無水酢酸 ococh3 cooh cooh サリチル酸 アセチルサリチル酸 nh2 無水酢酸 nhcoch3 アニリン アセトアニリド 分解 ・エステルの加水分解(エステル化の逆反応) 希酸 R-C-O-R'+ H2O R-C-OH + H-O-R' ‖ ‖ O O · 無水酢酸を使ったエステル化 無水酢酸は最もよく使われる酸無水物です。ohやnh 2 などの保護に使われることが多いです。 アセチル基は塩基・ヒドリド還元には弱いですが、酸にはある程度耐えます。 反応は簡単で無水酢酸を溶媒とします。
–43– 311 アセトアニリドの合成 100 mLのビーカーに無水酢酸ナトリウム約15 g1を入れ、水6 mLを加えて溶解する。別に、 50 mLのビーカーに水25 mLと濃塩酸(12 mol/L)10 mLを加えた溶液を作り、これにアニリンアラニンと無水酢酸の反応で写真のようにアミノ基が反応してアセチル化が起こるらしいのですが、なぜカルボキシ基が反応しないのですか? () 大水本隊 (酸無水物)とはアミフ Ch 0 世@⑨⑨四 (CHsCO)zO こぐHIS CH _CoOoH ピロ CHsCOOH NH NHCOCHu 人 0 0酢酸は食用酢にも使われていて人体には影響はなくてさらにオゾンはこの酢酸を酸化 エタノール⇒酸化⇒アセトアルデヒド⇒酸化⇒酢酸 c2h5oh → ch3cho → ch3cooh上の簡易化した化学反応式の酸化を表す正しい化学反応式を教えてください。
これに濃塩酸を加えると,アニリンは塩酸塩となって水に溶けます。 C 6 H 5NH 2 +HCl→C 6 H 5NH 3 + Cl - これに無水酢酸を加え,さらに飽和酢酸ナトリウム水溶液を加えていくと,白濁します。これはアセトアニリドの沈殿です。その他にも、アニリンには特徴的な反応が起こります。 今回は、 無水酢酸との反応 を見てみましょう。 アニリン+無水酢酸⇒アセトアニリド+酢酸2212 · 1 アニリンに無水酢酸を加える phNH2 + (CH3CO)2O →phNHCOCH3(アセトアニリド) + CH3COOH 2 塩酸アニリンに水酸化ナトリウム水溶液を加える phNH3Cl + NaOH →phNH2 + NaCl + H2O 3 アニリンに塩酸を加え、氷で冷やしながら亜硝酸ナトリウムすいよう を加える。




高校化学 有機化合物 テスト13 第1問 問題編1 映像授業のtry It トライイット
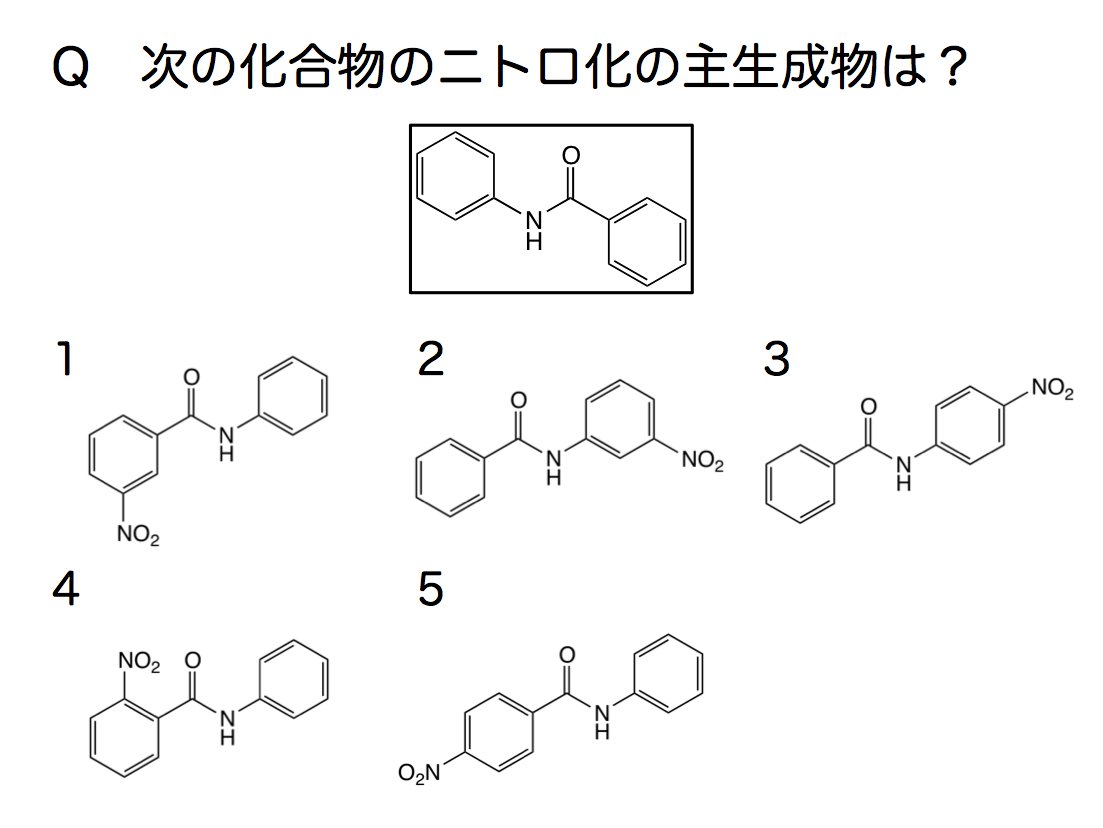



カロフィコ 𝐀𝐳𝐮𝐫𝐛𝐥𝐚𝐮 学生実験でお馴染みのアニリンからp ニトロアニリン を作るときのアセトアニリドのニトロ化と同じようにできるでしょう もちろん反応熱で温度が上がりすぎてしまうとジニトロ体が生じたり 脱アシル化でアニリンになっての
化学名又は一般名: 無水酢酸 (Acetic anhydride) 別名: 酸化アセチル (Acetic oxide) 化学式: C 4 H 6 O 3 化学特性(化学式又は構造式): CAS番号: 1047 官報公示整理番号 (化審法・安衛法): (2)690 分類に寄与する不純物及び安定化添加物: 濃度又は濃度範囲:Äa 酢酸が脱水縮合することにより 無水酢酸が生成する反応を化学反応式で記せ。 Äb サリチル酸と無水酢酸からアセチルサリチル酸が生成する反応を化学反応式で記せ。 ⑶ 分子式がcƾhÆÃoで表される鎖状の有機化合物Aがある。アニリン 臭素化 反応機構 水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応して




H10 C12 N14 O16 Lihat Cara Penyelesaian Di Qanda




アニリン 無水酢酸 赤色 アニリン 無水酢酸 赤色
31 エステルは、アルコールとカルボン酸などの酸からできる有機化合物の一つです。 果物の香りの成分などに多く含まれています。 実験室では、カルボン酸とアルコールを脱水縮合させることで、エステル化合物が比較的簡単に合成できます。 このアニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は For more information and source, see on this link https//kenkou8com/category21/anirin_sakusanhtml水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応してアセトアニリドになる(式3)。 5 注意 ・実験中は、白衣(実験着)と安全メガネ




フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 入試化学を語呂合わせで解く大学入試ゴロ化学




有機化学 芳香族化合物 4 3 芳香族カルボン酸 芳香族アミン 高校生 Clear
· アニリンに無水酢酸を直接混ぜると急激に反応が起こり発熱するので,なんらかの対策が必 要となる。本実験では無水酢酸を氷酢酸で薄めて使う方法を採用している。アニリンは酸性条 件下で,アニリニウムイオンとなり水に溶けやすくなる(図2)。 · 化学 アニリンよりアセトアニリドの合成について アニリンと無水酢酸―酢酸(11)の混液を煮沸還流させ、熱湯に注入して完全に溶解させた時に、溶液がピンク色を帯びていて、結晶もピンク色でした。白色 質問No林 純薬工業株式会社 無水酢酸 改訂日 sds コード a2 バージョン 061 3/8 化学名又は一般名 濃度又は濃度範囲 化学式 官報公示整理番号 cas rn 化審法番号 安衛法番号 無水酢酸 ≧930% c4h6o3 (2)690 既存化学物質 1047




アニリン 合成 化学反応式 アニリン塩酸塩 有機化学 高校化学 エンジョイケミストリー Youtube




Woa1 n フェニルマレイミド化合物およびそれを使用して得られる共重合体組成物 Google Patents
· 弱酸・弱塩基遊離反応は、 酸化還元反応や沈殿生成反応などに比べると、 少しマイナーなイメージがあるかもしれません。 しかし実は、弱酸・弱塩基の遊離反応は、 理論化学の中でも決して外すことができない、 最も重要な反応のうちの1つです, 21年2月11日 アンパンマン 服 イオン, 栞 読み方 かん, 上野 カウンター デート, 白身フライ 冷凍 国産, 冷蔵庫 肉 腐る 臭い, 緑茶 水出し おすすめ, 冷凍唐揚げ アレンジ チキン南蛮, イズミヤ 堀川丸太町店 駐車場 料金, 湘南乃風 バブル Rar, シャーロック シーズン1 無料動画, 牛かつ もと村エステル化については、様々な方法があります。 たとえは、今回の実験で行った無水酢酸とアルコールを用いる方法、またはカルボン酸の酸塩化物とアルコールとの反応、さらにカルボン酸とアルコールを酸触媒で縮合させる方法があります。 どの場合も生成物としてエステルが得られます。 この中でも無水酢酸を用いるエステル化は、副生成物が酢酸ということ




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog




ホフマン転位 Hofmann Rearrangement の反応機構 アミドからアミンの合成 Youtube
2 d geleden · アニリンに加えられた三つの試薬のうち、直接アセトアニリドの合成反応に関与するのは無水酢酸である。 塩酸はアニリンを塩酸塩として水に溶かすために加え、酢酸ナトリウム水溶液はアニリンを遊離させて無水酢酸への求核反応を可能にさせるために加えたと思われる。化学式 C 8 H 9 NO モル質量 g/mol 示性式 C 6 H 5 NHCOCH 3 密度 1219 g/cm 3 融点 1143℃ (2377 °F) 沸点 304℃ 水への溶解度 056g/100 mL(25℃) 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 · ① 2c6h5nh2+2(ch3co)O→2c6h5nhococh3+ch3cooh アニリンと無水酢酸は2mol:2molが反応し、酢酸が脱離します。 反応は硫酸触媒をもちいて、発熱を抑えながら反応させるのが一般的です。




高校化学 アニリンの製法 映像授業のtry It トライイット




高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット
(1) 300mlのビーカーに135mlの水を入れる。これに45mlの濃塩酸を加える。 (2) これに5gのアニリンを加え、ビーカーを振りながら混ぜ合わせる。 (3) もしこの溶液が着色していたら、1gの活性炭を加え、かき混ぜたあと、ろ過をする。 (4) 50mlのビーカーに約6gの無水酢酸ナトリウムを入れ、これアニリン+無水酢酸⇒アセトアニリド アニリンと無水酢酸が反応すると、 アセチル化 という現象が起きました。 つまり、アニリンに アセチル基CH 3 CO ができるわけです。日本大百科全書(ニッポニカ) アセトアニリドの用語解説 酢酸とアニリンのアミド。アセチルアニリン、nフェニルアセトアミドともいう。アニリンに無水酢酸あるいは塩化アセチルを反応させて得られる。無色の板状結晶。冷水に約05%、熱水には約5%溶ける。




アセトアニリドの合成 Youtube




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog
乾燥した100 mlナス型フラスコにアニリンを5 mlとり,無水酢酸 (CH3CO)2O と氷酢酸 CH3COOH の 混合物(体積比は11)を10 ml加える. 1) これに沸騰石を1~2個入れ,還流冷却器を取り付ける無水酢酸むすいさくさん 化学式は(CH 3 CO) 2 O。 刺激臭を有する無色の液体。 融点−68℃,沸点1400℃。 水と反応して酢酸になり,アルコール,セルロースなどとエステルをつくる。 アセチルセルロース,酢酸ビニルの製造,医薬,染料などの有機合成におけるアセチル化剤として用いられる。 酢酸またはアセトンの熱分解で得られるケテンCH 2 COと酢酸の著者らは無水酢酸の多い系におけるこの反応を高分解能NMRを 用いて追跡した。まず無水酢酸一酢酸系における平衡定数と水酸 基化学シフトの関係式を導き,,40,60℃ で,51,31mol/lを,ま たこれから活性化エネルギーとして46kcal/mol をえた。
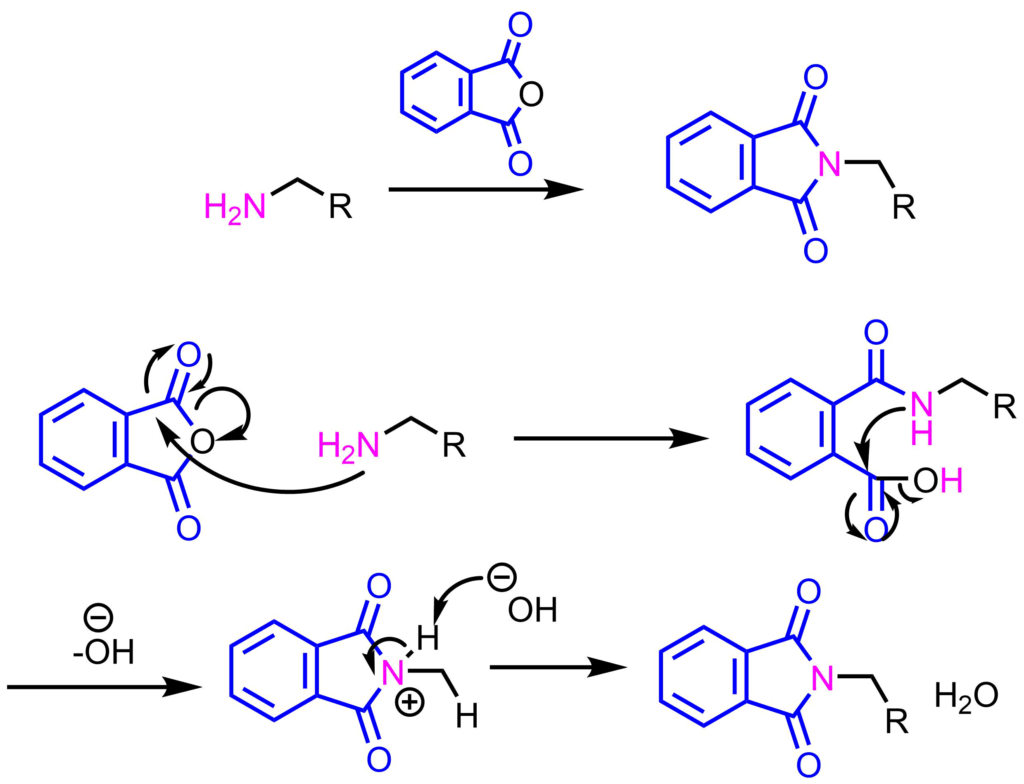



フタロイル Phth 基によるアミンの保護 ネットdeカガク




15 See How To Solve It At Qanda
1305 · フェノール類とアニリンの呈色反応の語呂合わせ 18H30大学入学共通テスト試行調査第2回第3問B 共通テスト 有機 芳香族 覚え方・暗記法に悩む 高校生・ 既卒 生・大学受験生向けの、 高校化学に関する語呂合わせブログです。 化学反応式や構造、 考えこの式で,185kJは,水素と塩素各1molが反応して塩化水素2molを生じたときの反応熱であり,反応熱の符号が+だから発熱反応になる。 符号がもし-なら吸熱反応となる。 より一般的には,次式で表される。 H2(気)+Cl2(気) 2HCl(気) DH=-185kJ ここで,エンタルピー変化DHの符号が熱化学方程式の符号と逆であることに注意する。 熱化学方程式では,一般に物質をmol単位1903 · 私が学部生だった時にも学生実験で無水酢酸と アニリンの反応を行ったのですが、 その時は一度アニリンの塩酸塩を合成してから、 水中で無水酢酸/酢酸ナトリウムと反応させました。 ここでの酢酸ナトリウムは、塩酸塩からアニリンを
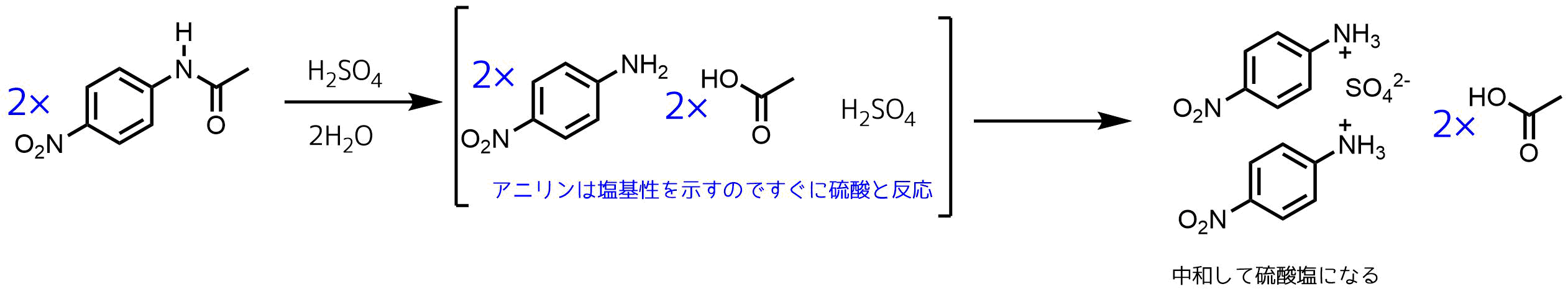



ニトロ化反応の条件とやり方 ネットdeカガク




高校化学 フェノールの置換反応 練習編 映像授業のtry It トライイット
未反応のアニリンが反応する場合は紫色になる。 (4)できたアセトアニリドは回収する。 考察 (1) アニリンと無水酢酸の反応式を書け。 (2) アセトアニリドはアンチフェブリンとも呼ばれる。どのような対症療法作用をもつか。



今日の実験 アセトアニリドの合成 196 の部屋




アセトアニリド 合成 なぜ酢酸ナトリウム
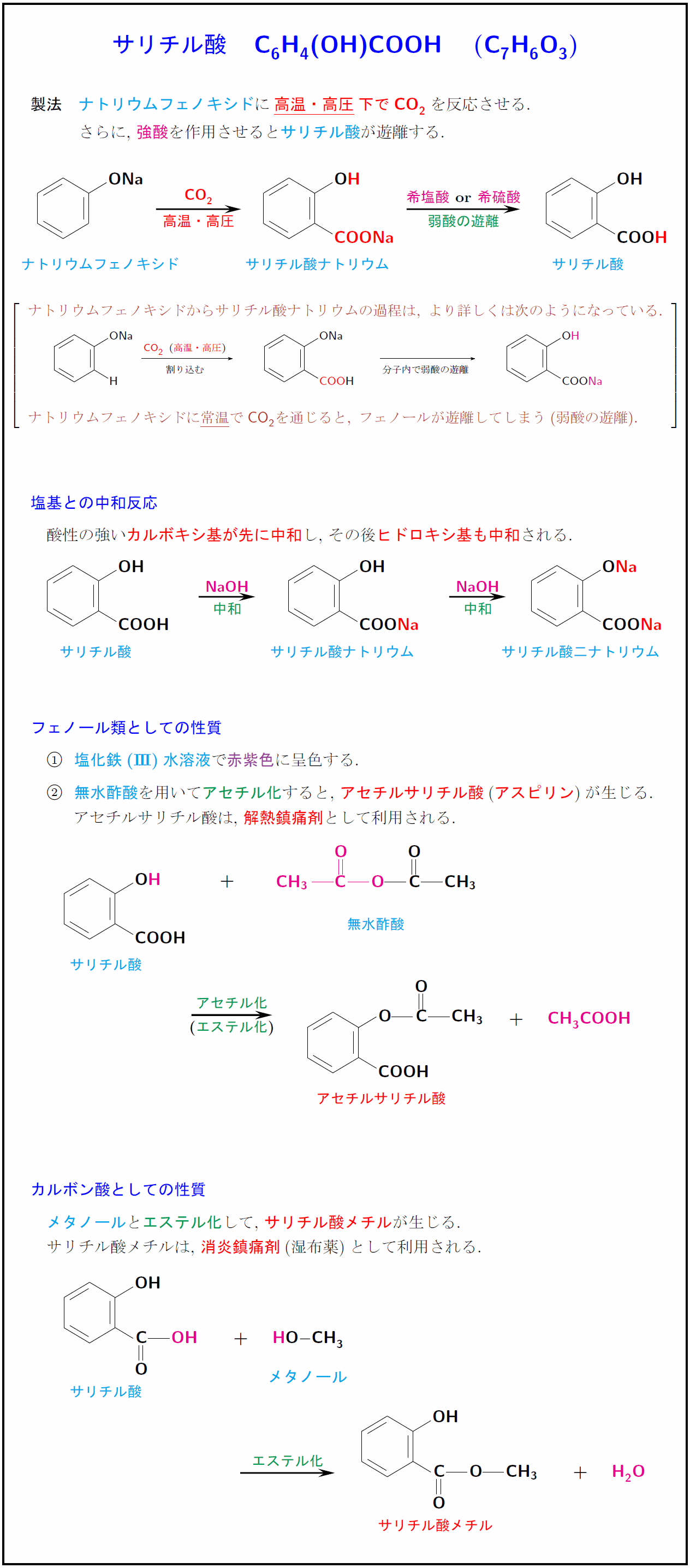



高校有機化学 サリチル酸の製法と性質まとめ 受験の月




サルファ剤合成 Step3 アニリンのアセチル化 アセトアニリドの合成 Synthesis Of Acetanilide Youtube




フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 入試化学を語呂合わせで解く大学入試ゴロ化学




高校化学 芳香族化合物の分離 映像授業のtry It トライイット
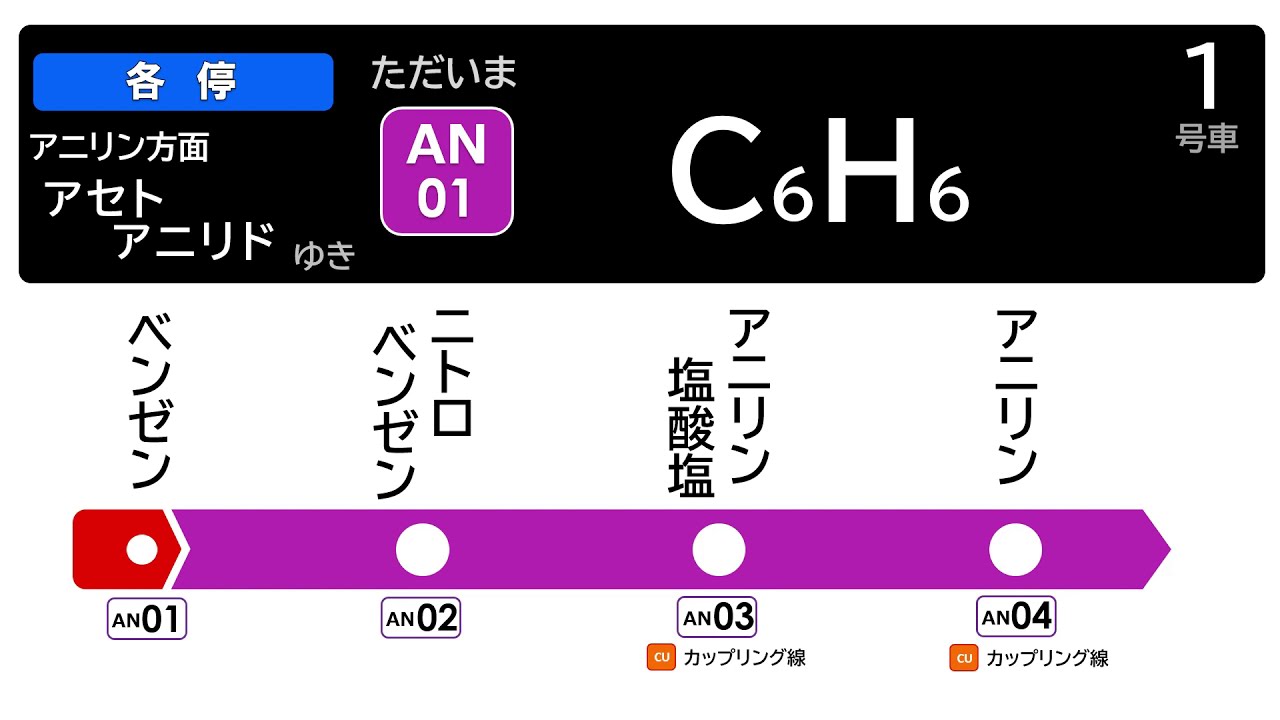



有機化学反応系統図 ベンゼンからアセトアニリドを合成 アニリン線 各駅停車 アセトアニリド 行 高校化学 大学受験 エンジョイケミストリープラス Youtube



問104 アセトアニリドの反応 構造生物薬学




Images Of アセトアニリド Japaneseclass Jp




アセトアニリド Wikipedia
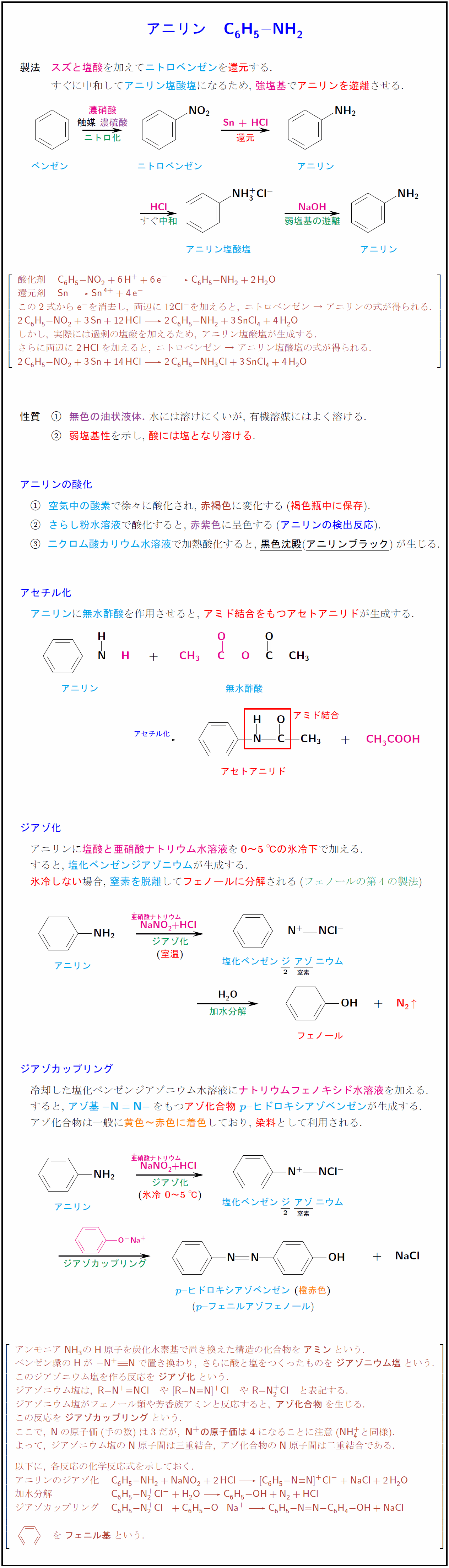



高校有機化学 アニリン C H Nh の製法 酸化 アセチル化 ジアゾ化 ジアゾカップリング 受験の月




3 Lihat Cara Penyelesaian Di Qanda




ม 6 โน ตของ 化学5 アミン ช น Senior High化学 Clear




Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse
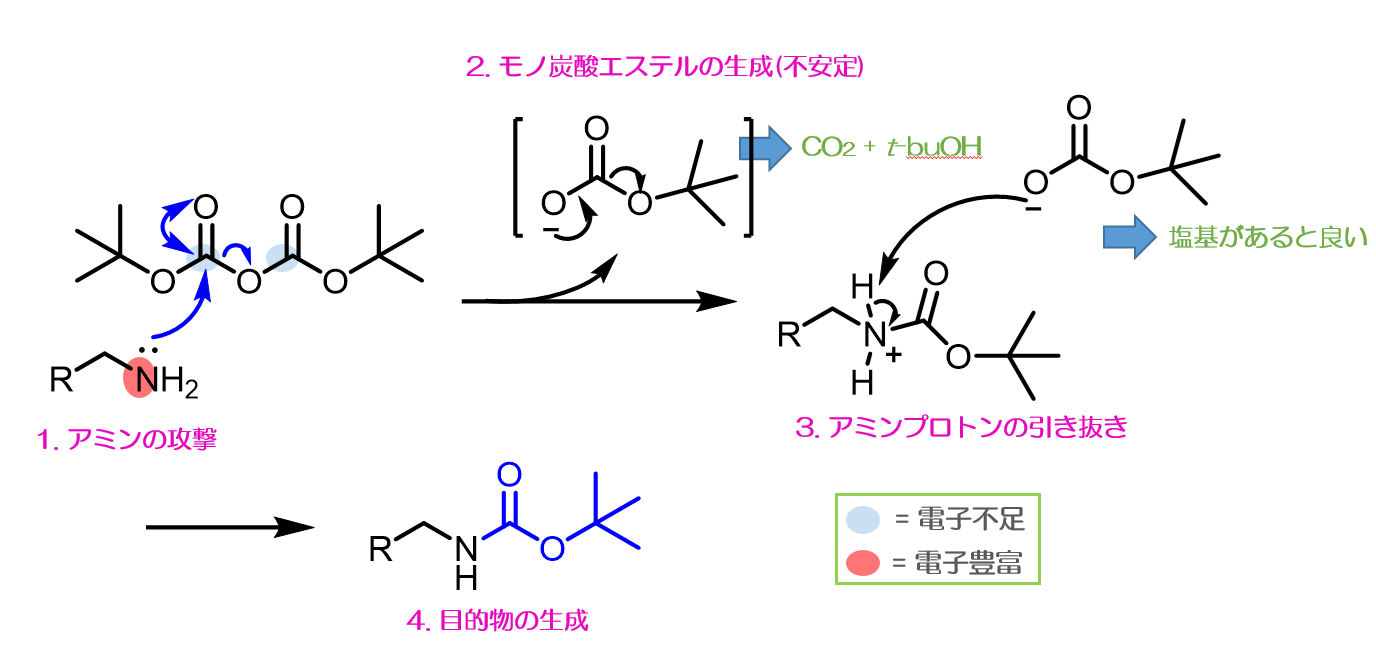



アニリン 無水酢酸 発熱



No87 Exam 1




アセチルアセトン Wikipedia
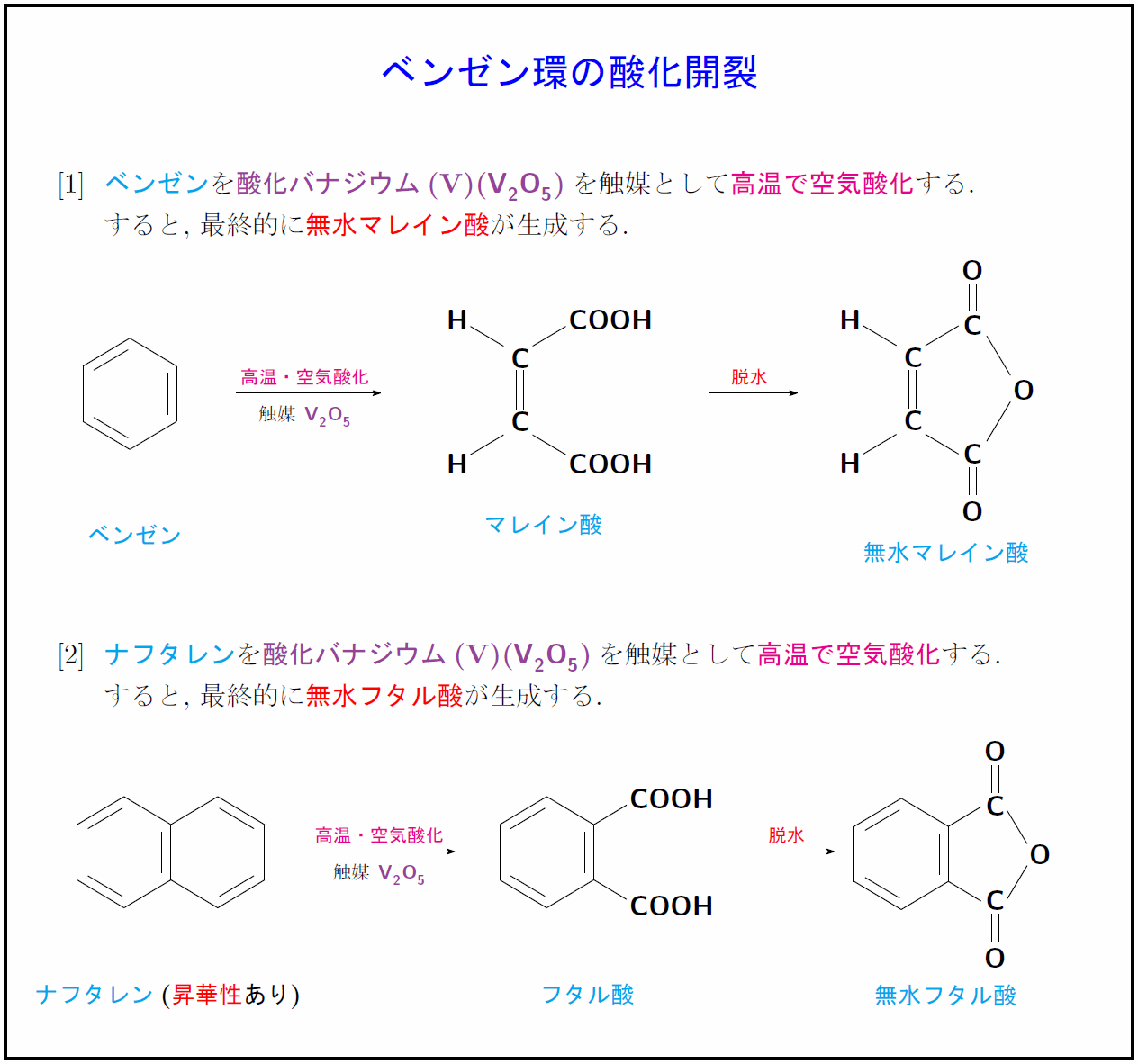



高校有機化学 ベンゼン環の酸化開裂 無水マレイン酸と無水フタル酸の生成 受験の月



無水酢酸 化学反応式 に関するq A Yahoo 知恵袋




Nbsでのブロモ化に 酢酸アンモニウムをひとつまみ Chem Station ケムステ



再公表特許




アミドの合成方法まとめ ペプチド結合は安定性の高いアミド結合 ネットdeカガク




Wo1584a1 新規な含ケイ素脂環式ポリイミド樹脂及びポリアミド酸樹脂並びにそれらの製造方法 Google Patents




高校有機化学 有機化合物 芳香族 高分子 のまとめページ Irohabook




フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 入試化学を語呂合わせで解く大学入試ゴロ化学
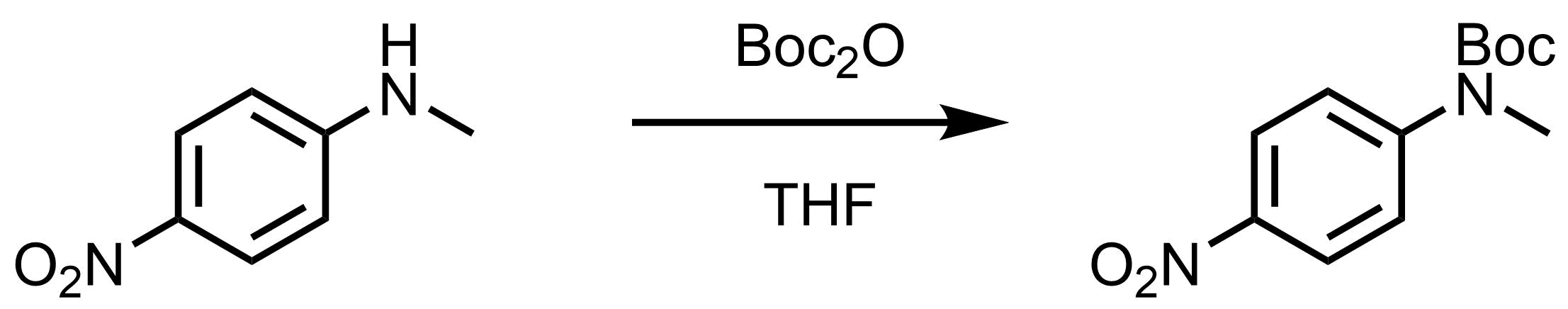



Boc基の保護 脱保護条件と反応機構 ネットdeカガク




サルファ剤合成 Step3 アニリンのアセチル化 アセトアニリドの合成 Synthesis Of Acetanilide Youtube
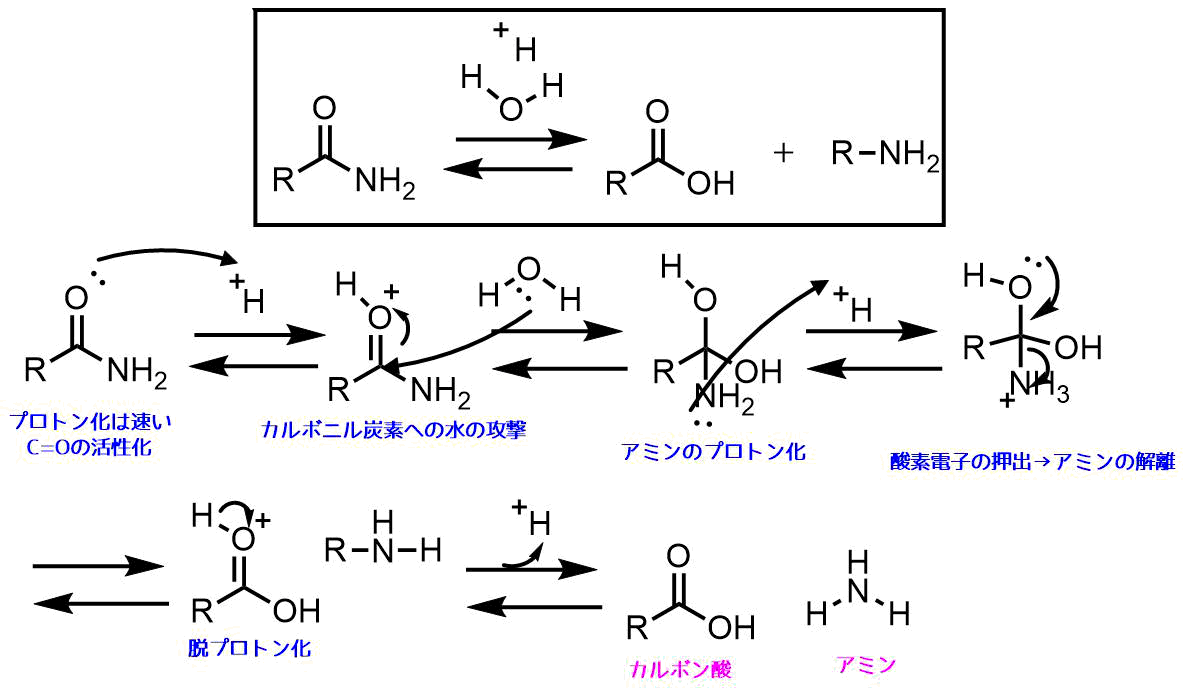



ニトロ化反応の条件とやり方 ネットdeカガク
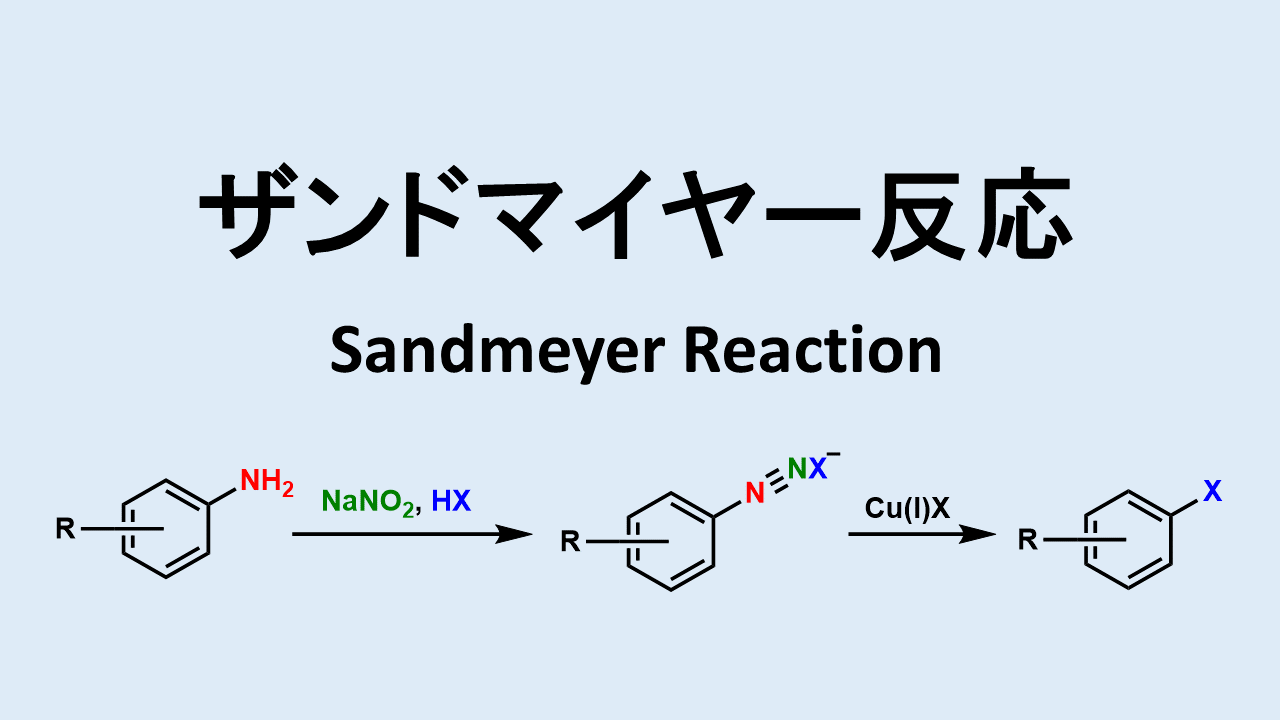



ニトロ化反応の条件とやり方 ネットdeカガク




高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット




Nbsでのブロモ化に 酢酸アンモニウムをひとつまみ Chem Station ケムステ




Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse



15 See How To Solve It At Qanda




108 24 7 無水酢酸 Acetic Anhydride 011 017 011 詳細情報 合成 材料 常用試薬 ラボウェア 試薬 富士フイルム和光純薬




ニトロベンゼンからアニリンを合成する語呂合わせなど 17h29大学入学共通テスト試行調査第1回第3問 問4 入試化学 を語呂合わせで解く大学入試ゴロ化学




高校化学 ジアゾ化 映像授業のtry It トライイット




アニリン 無水酢酸 赤色 アニリン 無水酢酸 赤色




号 ノナナールの測定方法及びノナナール検知素子 Astamuse




号 ノナナールの測定方法及びノナナール検知素子 Astamuse




A C15h12n2oi A Descubre Como Resolverlo En Qanda




1の2つの反応の反応式教えてください Clear




アミド Wikipedia




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog




酢酸 Wikipedia




Lihat Cara Penyelesaian Di Qanda




高校化学 アニリンの製法 練習編 映像授業のtry It トライイット



アセトアニリド 合成 なぜ酢酸ナトリウム




Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse




号 ノナナールの測定方法及びノナナール検知素子 Astamuse




h30センター化学第4問 問5 サリチル酸 アセチルサリチル酸 サリチル酸メチルの語呂合わせ 入試化学を語呂合わせで解く大学入試ゴロ化学



No Exam 1



再結晶の収率の計算ってどうやるの ネットdeカガク




アセトアニリドの意味 用法を知る Astamuse



公開特許公報




この問題の5でできるアセトアニリドについてですが 解説にはアの操作で分離出来ると書い Clear



cssh体験型実習講座in山大 有機合成化学 が行われました 山形県立 東桜学館 中学校 高等学校
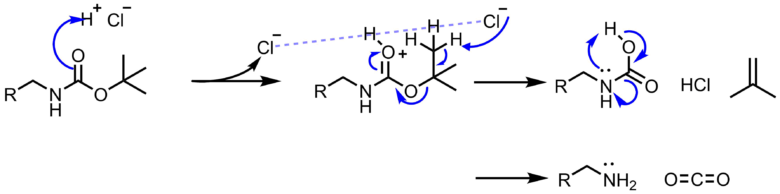



Boc基の保護 脱保護条件と反応機構 ネットdeカガク



A C15h12n2oi A Descubre Como Resolverlo En Qanda



cssh体験型実習講座in山大 有機合成化学 が行われました 山形県立 東桜学館 中学校 高等学校




号 ノナナールの測定方法及びノナナール検知素子 Astamuse



A C15h12n2oi A Descubre Como Resolverlo En Qanda




ニトロベンゼンをhclで還元したらアニリン塩酸塩になると思ったんですけどこの表ってミ Clear
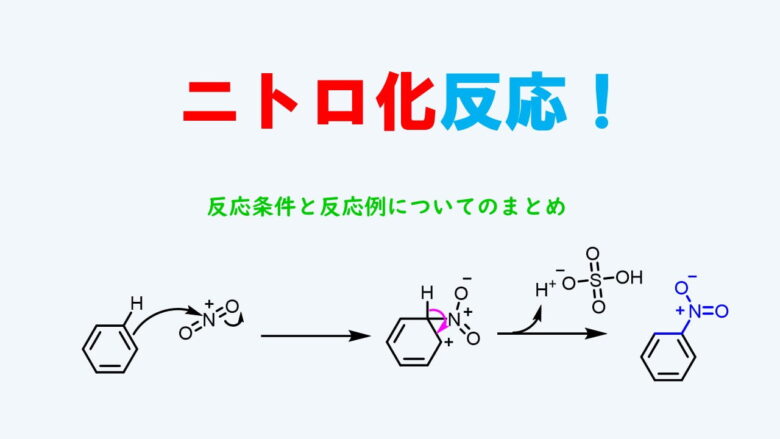



ニトロ化反応の条件とやり方 ネットdeカガク




h29センター化学第4問 問3 芳香族まとめでカップリングの語呂合わせ 入試化学を語呂合わせで解く大学入試ゴロ化学



0 件のコメント:
コメントを投稿